Iksuda Akan Mempresentasikan Analisis Awal Data Kanker Esofagus Dari Studi Fase 1 IKS014 di Simposium Kanker Gastrointestinal ASCO
Aktivitas anti-tumor yang menggembirakan terlihat di semua tingkat dosis dan dalam berbagai indikasi tumor
Tingkat manfaat klinis 80% untuk 10 pasien dengan kanker esofagus HER2+ yang telah menerima terapi sebelumnya yang mencakup komponen trastuzumab dalam setidaknya satu pengobatan sebelumnya
NEWCASTLE, Inggris–(BUSINESS WIRE)–Iksuda Therapeutics (Iksuda), pengembang antibody drug conjugates (ADC) terkemuka, hari ini mengumumkan presentasi analisis awal aktivitas pada pasien dengan kanker esofagus selama studi Fase 1 IKS014, ADC yang menargetkan human epidermal growth factor receptor 2 (HER2), pada pasien dengan tumor padat HER2+ lanjut, di Simposium Kanker Gastrointestinal ASCO 2026 di San Francisco, AS (8-10 Januari).
Studi Fase 1 (NCT05872295) adalah uji klinis non-acak, label terbuka, multisenter yang mengevaluasi IKS014 pada pasien dengan tumor padat lanjut lokal atau metastatik yang mengekspresikan HER2. Data dipresentasikan dari sub-populasi yang tidak direncanakan dari pasien dengan kanker esofagus dari bagian eskalasi dosis uji klinis yang dilakukan di Australia, yang dirancang untuk menetapkan dosis maksimum yang dapat ditoleransi dan/atau dosis fase 2 yang direkomendasikan untuk IKS014 sebagai monoterapi dan untuk memberikan data awal keamanan, tolerabilitas, kemanjuran, PK, PD, dan imunogenisitas.
Hingga Juli 2025, 62 pasien telah diobati dengan IKS014 di lima tingkat dosis (40, 60, 90, 120 dan 105 mg/m2), termasuk 10 pasien dengan kanker esofagus HER2+. Aktivitas anti-tumor yang menggembirakan terlihat di semua tingkat dosis pada pasien dengan berbagai indikasi tumor seperti kanker payudara, ovarium, kandung empedu, paru-paru dan esofagus, dan pada pasien dengan tumor HER2+ dan HER2 rendah.
Dari sub-kelompok 10 pasien dengan kanker esofagus HER2+, yang telah menerima terapi sebelumnya (median 3, rentang 1-6), lima mencapai respons, termasuk respons lengkap pada satu pasien dengan penyakit yang tidak dapat diukur, sementara tiga pasien lainnya menunjukkan penyakit stabil selama lebih dari enam bulan, menghasilkan tingkat manfaat klinis untuk IKS014 sebesar 80%. Hasil positif ini memerlukan eksplorasi lebih lanjut, dan bagian ekspansi dosis dari studi Fase 1 ini sekarang akan mencakup kohort ekspansi tambahan khusus untuk pasien dengan adenokarsinoma esofagus yang mengekspresikan HER2 yang sebelumnya telah menerima setidaknya satu lini pengobatan standar sebelumnya yang mungkin termasuk terapi yang diarahkan HER2.
Dr. Dave Simpson, Chief Executive Officer, Iksuda Therapeutics, berkomentar: "Tanda-tanda awal aktivitas dan tingkat manfaat klinis pada pasien dengan kanker esofagus lanjut yang telah diobati sangat menggembirakan. Ini adalah kanker yang terkenal sulit untuk diobati, dengan tingkat kelangsungan hidup yang relatif rendah dan toksisitas pengobatan yang tinggi. Kami berharap dapat terus mengeksplorasi potensi IKS014 untuk meningkatkan hasil klinis dalam kanker yang sulit diobati ini, serta di beberapa kanker pengekspresi HER2 lainnya."
Detail Presentasi Poster:
|
Judul Abstrak: |
Analisis awal aktivitas pada kanker esofagus selama eskalasi dosis fase 1 IKS014, antibody drug conjugate (ADC) yang menargetkan HER2, pada peserta dengan tumor padat HER2+ lanjut dan HER2 rendah |
|
|
Judul Sesi: |
Sesi Poster A: Kanker Esofagus dan Lambung dan Kanker Gastrointestinal Lainnya |
|
|
Tanggal/Waktu: |
9 Januari 2026, 02:30-04:30 WIB |
|
|
Lokasi: |
Level 1, West Hall |
|
|
Nomor Abstrak: |
355 |
Tentang IKS014
IKS014 adalah antibody drug conjugate terbaik di kelasnya yang potensial, mendapat manfaat dari aktivasi selektif tumor dan pelepasan agen sitotoksik monomethyl auristatin F (MMAF). Dalam uji praklinis, obat ini menunjukkan aktivitas yang mengesankan pada tumor yang mengekspresikan HER2 tinggi dan rendah dengan Indeks Terapeutik yang menguntungkan dibandingkan dengan obat yang diarahkan HER2 lainnya. Iksuda memperoleh hak eksklusif di seluruh dunia (tidak termasuk Tiongkok Raya dan Korea Selatan) untuk IKS014 dari LigaChem Biosciences (https://iksuda.com/2022/01/iksuda-deepens-clinical-pipeline/).
Tentang Iksuda Therapeutics: www.iksuda.com
Iksuda Therapeutics adalah perusahaan bioteknologi tahap klinis yang berbasis di Inggris yang berfokus pada pengembangan ADC terkemuka yang menargetkan tumor hematologis dan padat yang sulit diobati. Pipeline ADC Iksuda berpusat pada portofolio ADC prodrug yang memanfaatkan pelepasan selektif tumor dan aktivasi muatan dalam kombinasi dengan kimia konjugasi stabil termasuk platform PermaLink® miliknya. Pipeline awal menggabungkan kelas muatan alkilasi protein milik Iksuda, 'ProAlk . Konsep desain ADC Perusahaan sekarang telah divalidasi secara klinis untuk meningkatkan indeks terapeutik modalitas penting ini secara signifikan dan meningkatkan hasil untuk pasien yang hidup dengan kanker.
. Konsep desain ADC Perusahaan sekarang telah divalidasi secara klinis untuk meningkatkan indeks terapeutik modalitas penting ini secara signifikan dan meningkatkan hasil untuk pasien yang hidup dengan kanker.
Kontak
Untuk informasi lebih lanjut silakan hubungi:
Iksuda Therapeutics
Dave Simpson, Chief Executive Officer
Tel: +44 (0) 191 6031680
[email protected]
FTI Consulting (Media Keuangan dan IR)
Simon Conway / Rob Winder / Amy Byrne
Tel: +44 (0) 020 3727 1000
[email protected]
Anda Mungkin Juga Menyukai
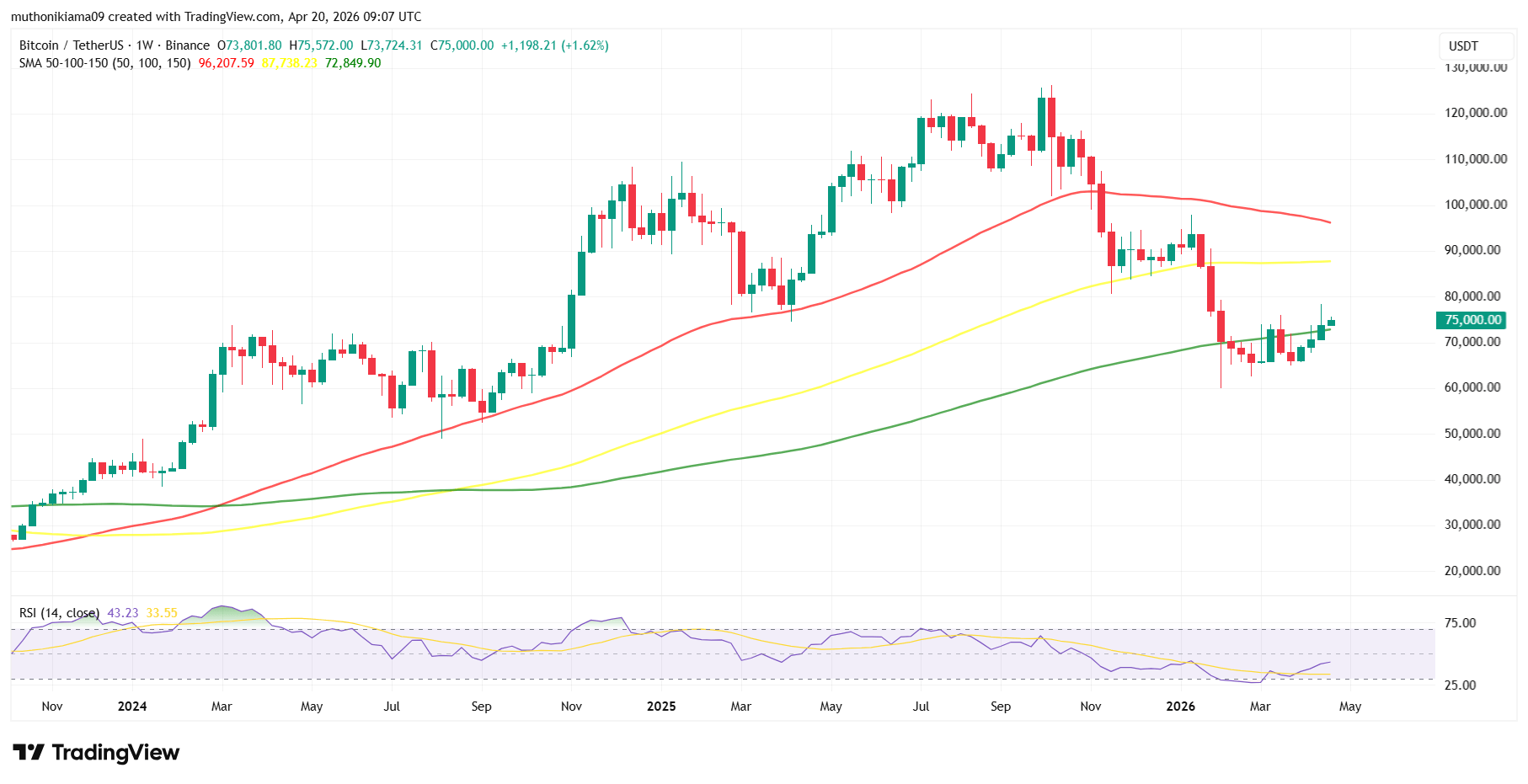
BTC, ETH, XRP Bersiap! Data Ekonomi AS Bakal Jadi Penentu
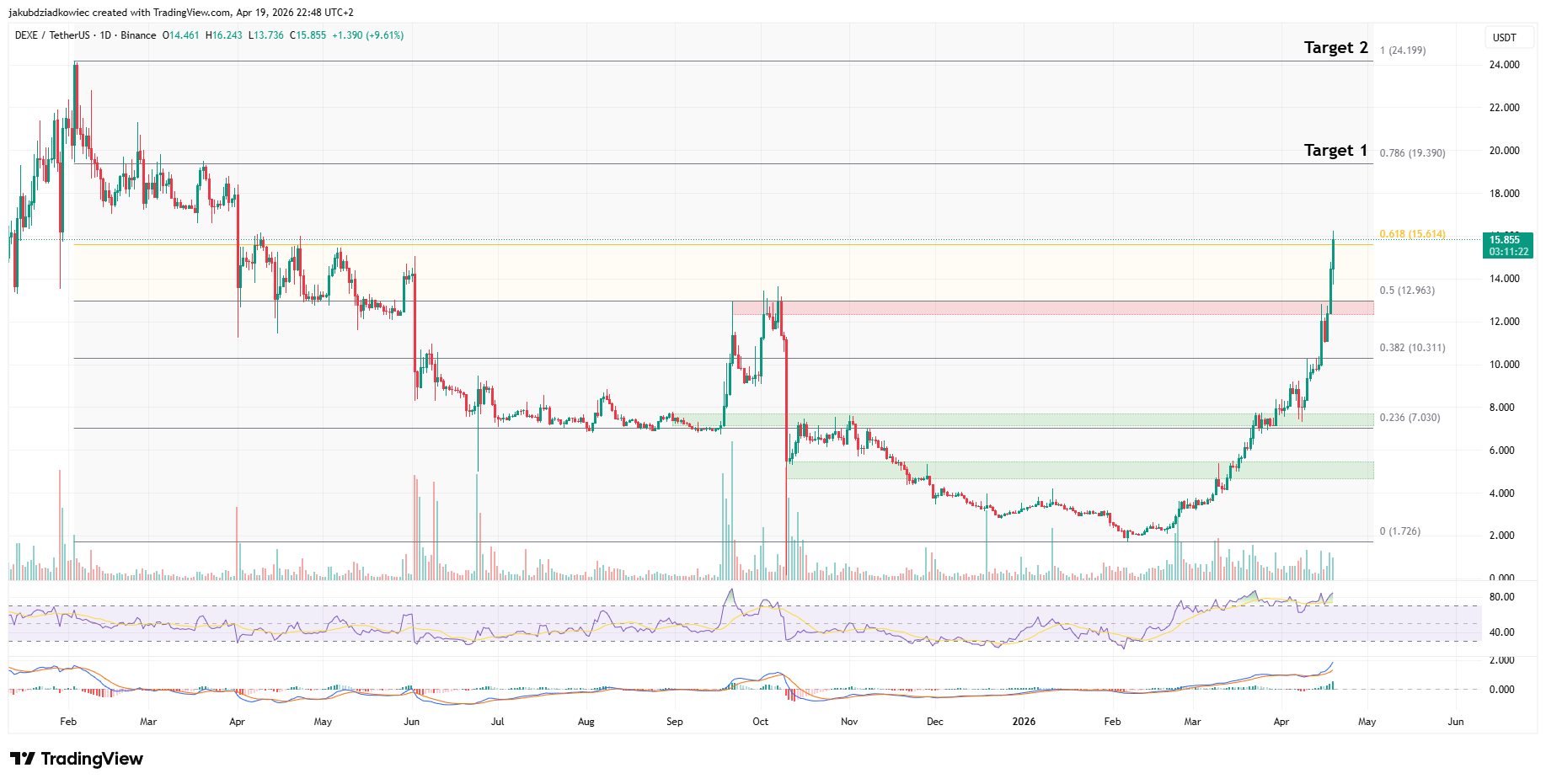
3 Altcoin Potensial Pekan Ini: DEXE, ENA, dan MemeCore